 Ripresa vegetativa e mobilitazione delle riserve
Ripresa vegetativa e mobilitazione delle riserve
Con l’arrivo della primavera e il superamento della stasi invernale, l’olivo riprende il proprio ciclo annuale. Alla ripresa vegetativa, la pianta mobilita le riserve energetiche accumulate negli organi legnosi (branche, tronco e radici) sotto forma di amido, derivanti dalla conversione dell’energia solare in energia chimica mediante la fotosintesi dell’anno precedente.
Con l’aumento delle temperature e della domanda metabolica, le riserve di amido vengono idrolizzate dagli enzimi alfa- e beta-amilasi, liberando zuccheri solubili costituiti prevalentemente da saccarosio e mannitolo. Questi composti, attraverso il floema, vengono traslocati verso le gemme in fase di schiusura, sostenendo la formazione e lo sviluppo dei germogli fino al raggiungimento della piena autonomia fotosintetica da parte della nuova porzione di chioma.
Durante la fase fenologica iniziale, le gemme vegetative generalmente si schiudono prima di quelle fiorali. Questo fenomeno, noto come eterocronia tra germogliamento e mignolatura, riflette la priorità metabolica della pianta nel ripristinare l’apparato fogliare. Le gemme vegetative, essendo strutturalmente più semplici e fisiologicamente meno esigenti, richiedono un apporto minore di risorse energetiche e stimoli ormonali rispetto a quelli fiorali, favorendo il loro risveglio anticipato. In questo modo, la pianta mobilita efficacemente le riserve energetiche, preparandosi alla successiva e più dispendiosa fase della fioritura.
Morfologia dei fiori
La mignolatura segna la conclusione dei processi di induzione (biochimica) e differenziazione (anatomica) fiorale, non visibili a occhio nudo, e corrisponde allo sviluppo delle strutture che daranno origine ai fiori, riuniti in infiorescenze paniculate (pannocchie), comunemente denominate mignole.

L’olivo (Olea europaea) è considerato una specie andromonoica, in quanto sulla stessa pianta produce sia fiori ermafroditi (perfetti) sia fiori staminiferi (maschili), nei quali il pistillo abortisce in diverse fasi dello sviluppo (Cuevas & Polito, 2004).


I fiori ermafroditi possiedono entrambi gli organi sessuali: il pistillo (gineceo), che costituisce l’apparato femminile, e due stami, che rappresentano l’apparato maschile. Il pistillo comprende una porzione basale ampia e rotondeggiante chiamata ovario, lo stilo (breve prolungamento dell’ovario) e lo stigma, situato all’apice, bifido e ricco di papille, che aumentano la superficie di contatto per accogliere il polline e favorirne la germinazione.
Lo stame (androceo) è costituito dal filamento che sostiene l’antera, deputata a produrre i granuli di polline e a rilasciarli al momento della sua apertura (deiscenza longitudinale).

Il polline si forma nelle sacche polliniche (generalmente quattro), situate all’interno delle due teche (o logge) che compongono l’antera tipicamente bilobata. Le sacche polliniche (microsporangi) sono rivestite internamente dal tapetum, tessuto specializzato fondamentale per il nutrimento dei granuli di polline in via di sviluppo e per la sintesi della parete pollinica.
Formazione del polline (microsporogenesi)
Circa un mese prima dell’apertura del fiore, all’interno delle antere si trovano le cellule madri del polline (microsporociti), diploidi, con corredo cromosomico caratteristico della specie: 2n = 46 cromosomi (Cruz et al., 2016), organizzati in 23 coppie omologhe, ciascuna composta da un cromosoma di origine paterna e uno di origine materna.
Ogni microsporocita va incontro alla meiosi, una particolare divisione cellulare riduzionale tipica delle cellule della linea germinale.
Attraverso questo processo, che inizia circa 20–25 giorni prima dell’apertura del fiore (antesi), si originano quattro cellule figlie aploidi, dette microspore, ciascuna con n = 23 cromosomi singoli, cioè la metà del numero di cromosomi della cellula madre.
Inizialmente, queste quattro cellule restano unite, formando una struttura detta tetrade di microspore, avvolta da una parete protettiva di callosio.
La meiosi, fondamentale per la riproduzione sessuata, consente il mantenimento costante del numero di cromosomi tra le generazioni. Infatti, se durante questo processo meiotico il corredo cromosomico non venisse dimezzato, a ogni fecondazione, con la fusione dei gameti maschili e femminili, il numero di cromosomi raddoppierebbe.
Inoltre, durante la profase I della meiosi, avviene un mescolamento genetico chiamato crossing-over, che aumenta la variabilità genetica e contribuisce all’adattamento e alla sopravvivenza della specie.
Per questo motivo, l’olivo predilige l’impollinazione incrociata tra esemplari diversi della stessa specie, considerata prevalentemente allogama.
La parete di callosio che avvolge la tetrade svolge una funzione protettiva temporanea: isola le quattro microspore neoformate e ne impedisce la fusione.
Successivamente, grazie all’azione di enzimi callasi prodotti dal tapetum, il callosio viene degradato, consentendo la liberazione delle singole microspore nella sacca pollinica.
Microgametogenesi
Ciascuna microspora aploide va incontro a una prima divisione mediante mitosi asimmetrica, generando due cellule: una più grande, detta cellula vegetativa e una più piccola, detta cellula generativa, racchiuse nella parete pollinica (sporoderma), costituita da intina all’interno ed esina all’esterno.
Durante questa fase di maturazione, il tapetum va incontro a morte cellulare programmata (Programmed Cell Death, PCD), rilasciando sulla superficie dei granuli pollinici il “pollen coat”, una sostanza viscosa di colore giallastro costituita prevalentemente da lipidi, carotenoidi, composti fenolici, proteine e carboidrati.
Il pollen coat, che ricopre l’esina, svolge diverse funzioni biologiche fondamentali: protegge il granulo pollinico dalla disidratazione, dalle radiazioni UV e dai patogeni; inoltre favorisce i processi di riconoscimento reciproco tra polline e stigma, facilita l’idratazione del granulo e l’avvio della germinazione del tubetto pollinico (Pacini & Hesse, 2005).
L’esina, composta da sporopollenina, una delle sostanze biologiche più resistenti in natura, presenta aperture germinative (colpi e pori) attraverso le quali, l’intina della cellula vegetativa si estrude dando origine al tubetto pollinico.
Durante la germinazione del polline sullo stigma e l’allungamento del tubetto pollinico verso l’ovulo, la cellula generativa subisce una seconda divisione mitotica, dando origine ai due gameti maschili aploidi.
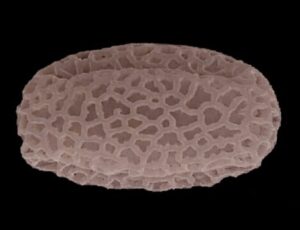
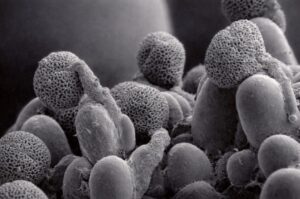
Il polline dell’olivo è tricolporato, caratterizzato cioè da tre solchi longitudinali (ectoaperture), detti colpi, disposti simmetricamente lungo l’asse equatoriale del granulo pollinico, ciascuno provvisto di un poro interno (endoapertura). I granuli, di forma sferoidale-subprolata, rimangono di dimensioni medio-piccole (circa 20–22 µm), e possono variare leggermente tra le diverse cultivar.
La struttura tricolporata, associata a un’esina reticolata, rende i granuli leggeri e resistenti, proteggendoli dalla disidratazione e facilitandone il trasporto anemofilo.
Germinazione, fecondazione e incompatibilità
Una volta raggiunto lo stigma, il polline compatibile germina grazie all’idratazione e ai nutrienti forniti dagli essudati stigmatici (Rejón et al., 2016).
Il tubetto pollinico, penetrando lungo lo stilo, trasporta le due cellule spermatiche fino all’ovulo. Attraverso il micropilo raggiunge il sacco embrionale, dove avviene la doppia fecondazione: una cellula spermatica si fonde con la cellula uovo formando lo zigote diploide (2n), mentre l’altra si unisce ai due nuclei polari (n+n) della cellula centrale, dando origine all’endosperma triploide (3n), un tessuto nutritivo che sosterrà lo sviluppo dell’embrione.
In molte cultivar di Olea europaea, la fecondazione è regolata da meccanismi di auto-incompatibilità diallelica (Diallelic Self-Incompatibility, DSI), che inibiscono la germinazione o lo sviluppo del tubetto pollinico sugli stigmi dello stesso genotipo o di genotipi appartenenti allo stesso gruppo di incompatibilità. Studi recenti hanno evidenziato un sistema diallelico secondo cui le cultivar sono classificate principalmente in due gruppi genetici, G1 e G2, nei quali le cultivar appartenenti allo stesso gruppo generalmente non si fecondano tra loro (Mariotti et al., 2020, 2021).
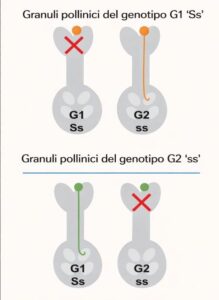
Sebbene alcune cultivar presentino una parziale auto-fertilità (pseudo-self-compatibility; Alagna et al., 2019), l’olivo è prevalentemente allogamo. La presenza di cultivar impollinatrici compatibili, appartenenti a gruppi differenti (G1 e G2), è essenziale per ottenere un’allegagione ottimale. Tuttavia, affinché l’impollinazione sia efficace è necessario che le cultivar fioriscano contemporaneamente e che il polline sia vitale e capace di germinare, condizioni fondamentali per garantire una regolare fruttificazione.
Nota finale: studi recenti indicano che il sistema DSI dell’olivo potrebbe essere più
complesso del modello diallelico semplice, mostrando alcune caratteristiche simili a un
sistema sporofitico non convenzionale (“unconventional homomorphic sporophytic diallelic
system”) (Cuevas et al., 2024).
Bibliografia:
- Cuevas, J., Polito, V.S. (2004). Self- and cross-incompatibility in olive (Olea europaea L.):
Pollen–pistil interactions and fruit set. Annals of Botany, 93(2), 257–264. - Cuevas, J., Chiamolera, F.M., Pinillos, V., Rodríguez, F., Salinas, I., Cabello, D., Arbeiter,
A.B., Bandelj, D., Božiković, M.R., & Selak, G.V. (2024). Backcrossing failure between
‘Sikitita’ olive and its male parent ‘Arbequina’: Implications for the self-incompatibility system
and pollination designs of olive orchards. Plants, 13, 2872. - Mariotti, R., Fontanella, F., Baldoni, L. (2020). Diallelic self-incompatibility in olive: Group
assignment and implications for orchard management. Plants, 9(8), 1010. - Mariotti, R., Fontanella, F., Baldoni, L. (2021). Pollen–pistil interactions and compatibility
groups in olive cultivars: Advances in understanding DSI. Horticulturae, 7(4), 93. - Pacini, E., Hesse, M. (2005). Pollenkitt – Its composition, forms and functions. Plant
Systematics and Evolution, 250(1-4), 1-14. - Rejón, J. D., Delalande, F., Schaeffer-Reiss, C., Alché, J. D., Rodríguez-García, M. I., Van
Dorsselaer, A., Castro, A. J. (2016). The pollen coat proteome: At the cutting edge of plant
reproduction. Proteomes, 4(1), 5.
Crediti fotografici:
Foto 2 e 3: Dott. Matteo Zucchini, presente come Figure 4 nella sua PhD Thesis “Growth control and productive aptitude of Olive tree (Olea europaea L.)”, Università Politecnica delle Marche, Academic year 2022-2023
Foto 4: Olea – Trattato di olivicoltura”, a cura di Piero Fiorino, Edagricole, 2020, Fig. 3.7)
Foto 5: Olea – Trattato di olivicoltura, a cura di Piero Fiorino, Edagricole, 2020, Fig. 3.7.
Foto 6: J. Cuevas in “Why Olive Produces Many More Flowers Than Fruit?”, Posted Date: 19 November 2024, doi: 10.



















