 Sono quasi venti anni (Fu J. 2003) che si studia come, l’introduzione dell’acido oleico nella dieta, possa aiutare a controllare il “senso di fame” attivando un processo ormonale fisiologico.
Sono quasi venti anni (Fu J. 2003) che si studia come, l’introduzione dell’acido oleico nella dieta, possa aiutare a controllare il “senso di fame” attivando un processo ormonale fisiologico.
Da molti anni si è appurato che, l’acido oleico, una volta che ha raggiunto l’intestino, viene trasformato in un ormone lipidico, l’oleoiletanolamide (OEA) che sarebbe in grado di agire su un tipo di recettore nucleare chiamato PPARa (Peroxisome Proliferator Activated Receptor Alpha) capace di inibire lo stimolo della fame, contemporaneamente di aumentare la combustione dei grassi e di diminuire l’accumulo di grasso, cosa che non si verifica quando vengono ingerite proteine o carboidrati.
Già ad ottobre 2008 e luglio 2014, avevo pubblicato due articoli, che oggi integro avendo a disposizione risultati di numerose ricerche tali da poter fare il punto sulla situazione, anche perché siamo passati dalla ricerca su animale di laboratorio all’uomo tanto da essere disponibile l’OEA, anche come integratore.
L’OEA si trova in piccolissima quantità, nell’ordine dei microgrammi, nell’avena, nel cacao e nelle noci, ma è l’intestino tenue che sintetizza questo composto in quantità significative.
Con un maggiore consumo di alimenti contenenti acidi grassi monoinsaturi, per esempio l’olio d’oliva, l’avocado e le noci, le concentrazioni ematiche di OEA aumentano.
L’OEA è un “endocannabinoide”, cioè una sostanza endogena che interagisce con i recettori cannabinoidi deputati alla modulazione dell’eccitabilità neuronale.
Secondo una teoria, già formulata negli anni novanta, l’OEA impedisce ad un altro endocannabinoide, l’arachidonietanolamina (endocannabinoide anandammide) di legarsi al recettore cannabinoide di tipo 1, il CB1R. Poiché l’Arachidonietanolamina stimola l’appetito attraverso l’interazione con il CB1, l’OEA, agendo come un agonista / antagonista, riduce l’appetito. L’effetto dell’OEA è stato definito “anoressizzante” perché aumenta la sazietà anche tra i pasti.
L’OEA riduce l’assunzione di cibo, oltre i percorsi della dopamina edonica, anche attivando i circuiti cerebrali omeostatici dell’ossitocina e dell’istamina. Ci sono prove che l’OEA può anche attenuare la segnalazione del recettore 1 dei cannabinoidi edonici (CB1R), la cui attivazione è associata ad un aumento dell’assunzione di cibo. Infine l’OEA riduce il trasporto dei lipidi negli adipociti al fine di diminuire la massa grassa.
L’OEA diminuisce durante il digiuno e aumenta dopo i pasti; praticamente la produzione di OEA, nell’intestino tenue, funge da “sensore molecolare” che collega l’assunzione dei grassi alla sazietà.
Quando i ricercatori hanno analizzato i campioni ematici dei soggetti in studio, prelevati prima e dopo la somministrazione di OEA, hanno osservato che questo supplemento aveva attivato il gene PPAR-alfa, riducendo l’appetito. Il recettore PPAR-alfa nell’intestino svolge un ruolo nella stimolazione dei nervi vaghi, creando sazietà nel nucleo paraventricolare dell’ipotalamo attraverso il nucleo del tratto solitario bulbare.
La somministrazione di OEA, rispetto ai controlli, ha determinato il miglioramento delle misure antropometriche (peso, Body Mass Index (BMI), circonferenza vita e massa grassa), sensazioni di sazietà / appetito (fame, desiderio di consumare cibo, diminuita voglia di dolci e aumentata sensazione di pienezza).
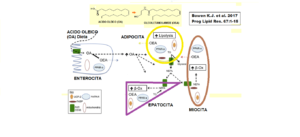
L’acido oleico, dopo l’assunzione, entra all’interno degli enterociti attraverso il recettore FAT/CD36 venendo poi trasformato in OEA.
L’OEA agisce:
1) sugli adipociti aumentando la lipolisi attivando PPAR-alfa;
2) sui miociti aumentando la beta ossidazione dei grassi liberi (NEFA);
3) sugli epatociti aumentando la beta ossidazione degli acidi grassi liberi.
Questi tre tipi cellulari liberano OEA.
Un recente lavoro del 2020, ha dimostrato che l’OEA attiva, oltre l’espressione dei geni PPAR-alfa, anche quelli delle proteine di disaccoppiamento 1 e 2 (UCP1 e UCP2) nelle cellule mononucleate del sangue periferico (PBMC). Questo lavoro ha permesso di dimostrare il ruolo valido dell’OEA nelle malattie del fegato (steatosi epatica).
Nel gruppo di pazienti trattati con OEA è stata osservata anche una diminuzione significativa degli indici antropometrici, degli apporti energetici e di carboidrati, dei parametri glicemici, ad eccezione della concentrazione di emoglobina A1c, rispetto al gruppo placebo.
Il trattamento con OEA ha determinato significativamente una diminuzione dei livelli sierici di trigliceridi, delle transaminasi e un aumento del colesterolo lipoproteico ad alta densità (HDL-C colesterolo buono).
È importante sottolineare che un miglioramento significativo dei livelli di trigliceridi, transaminasi (ALT, AST), HDL-C e delle sensazioni di appetito da parte dell’OEA era sotto l’influenza dell’indice di massa corporea (BMI).
In conclusione, il presente studio, per la prima volta, ha rivelato che l’integrazione di OEA ha migliorato significativamente i fattori di rischio antropometrici e metabolici legati alla steatosi epatica non alcolica (NAFLD, Nonalcoholic Fatty Liver Disease) abbastanza diffusa nella popolazione (documentata ecograficamente in oltre il 25% degli italiani con una percentuale maggiore negli anziani, soggetti sovrappeso, nei diabetici e negli obesi).
Per concludere, ancora una volta è possibile affermare come l’utilizzo regolare di Olio Extravergine di Oliva sia importante per il buon funzionamento di molti processi metabolici del nostro organismo.
Bibliografia
Fu J. et al. 2003 Oleylethanolamide regulates feeding and body weight through activation of the nuclear receptor PPAR-alpha. Nature, 425: 90-93
Mennella I. et al. 2015, Oleic acid content of a meal promotes oleoylethanolamide response and reduces subsequent energy intake in humans. Food Funct. 204-10.
Bowen K.J. et al. 2017, Oleic acid-derived oleoylethanolamide: A nutritional science perspective. Prog Lipid Res. 67:1-15
Laleh P. et al. 2018, Oleoylethanolamide increases the expression of PPAR-Α and reduces appetite and body weight in obese people: a clinical trial. Appetite. 128, 44‐49
Tutunchi H. et al. 2020, Oleoylethanolamide supplementation in obese patients newly diagnosed with non-alcoholic fatty liver disease: Effects on metabolic parameters, anthropometric indices, and expression of PPAR-α, UCP1, and UCP2 genes. Pharmacol Res., 156:104770.
Romano A. et al. 2020, Oleoylethanolamide decreases frustration stress-induced binge-like eating in female rats: a novel potential treatment for binge eating disorder. Neuropsychopharmacology; 45:1931–41. Già pubblicato qui.
Sfoglia gratuitamente l’Olivo News cliccando qui



















